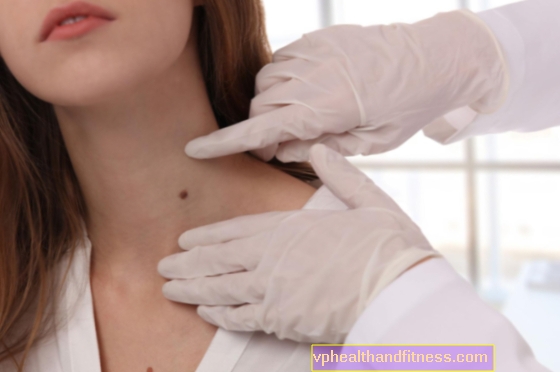
1 viaal sisaldab nominaalselt 250 RÜ, 500 RÜ või 1000 RÜ inimese VIII hüübimisfaktor. See ravim sisaldab naatriumi (alla 1 mmol (23 mg) / viaal 250 RÜ, kuni 1,75 mmol (40 mg) / viaal 500 RÜ ja kuni 1,75 mmol (40 mg / viaal 1000 RÜ).
| Nimi | Pakendi sisu | Toimeaine | Hind 100% | Viimati muudetud |
| Oktaanaat | 1 viaal 1000 RÜ + valmistamiseks lahustamine, pulber ja lahustamine lahendus šoki jaoks ja / või inf. | VIII faktor | 2019-04-05 |
Tegevus
Hemorraagiline ravim, vere hüübimisfaktor VIII. VIII hüübimisfaktor eksisteerib von Willebrandi faktoriga (FVIII ja vWF) koosneva bimolekulaarse kompleksina, millel on erinevad füsioloogilised funktsioonid. Hemofiiliaga patsientidele manustamisel seondub VIII faktor patsiendi vereringes von Willebrandi faktoriga. Aktiivne VIII tegur toimib aktiivse IX teguri kofaktorina, kiirendades X teguri muundumist aktiivseks teguriks X. Aktiivne tegur X muudab protrombiini trombiiniks. Seejärel muudab trombiin fibrinogeeni fibriiniks, mis võimaldab trombil tekkida. Pärast preparaadi süstimist jääb vereringesse umbes 2/3 kuni 3/4 VIII faktorit. Plasmas saavutatud VIII faktori aktiivsuse tase peaks olema vahemikus 80% kuni 120% prognoositavast VIII faktori aktiivsusest. VIII faktori aktiivsus plasmas väheneb kahefaasilises eksponentsiaalses jaotuses. Esialgses faasis on jaotumine intravaskulaarsete ja muude kambrite (kehavedelike) vahel plasma eliminatsiooni poolväärtusajaga 3 kuni 6 tundi. Järgmises aeglasemas faasis, mis peegeldab tõenäoliselt VIII faktori tarbimist T0,5, on 8 kuni 20 tundi. .
Annustamine
Intravenoosselt ei tohi manustada rohkem kui 2-3 ml / min. Annused ja asendusravi kestus sõltuvad VIII faktori puudulikkuse raskusastmest, verejooksu kohast ja ulatusest ning patsiendi kliinilisest seisundist. Manustatud VIII faktori ühikute arv on väljendatud rahvusvahelistes ühikutes (RÜ), mis on WHO heakskiidetud VIII faktori preparaatide praegune standard. VIII faktori aktiivsus plasmas väljendatakse kas protsentides (inimese normaalse plasma suhtes) või RÜ-des. vastavalt VIII faktori plasmakontsentratsioonile. 1 RÜ VIII faktori aktiivsus on samaväärne VIII faktori kogusega 1 ml normaalse inimese plasmas. VIII faktori vajaliku annuse arvutamine põhineb empiirilistel andmetel, et 1 RÜ faktor VIII / kg suurendab plasma VIII faktori aktiivsust 1,5–2% võrra normaalsest aktiivsusest. Vajalik annus määratakse järgmise valemi abil: vajalik ühikute arv = kuu. (kg) x vajalik VIII faktori tõus (%) (RÜ / dL) x 0,5. Manustamise kogust ja sagedust tuleb individuaalselt kohandada. Varajane verejooks liigestesse, lihastesse või suhu: vajalik VIII faktori tase on 20–40% normist, infusiooni tuleb korrata iga 12–24 tunni järel, vähemalt ühe päeva jooksul, kuni verejooksu põhjustatud valu on möödas või haav on paranenud. Ulatuslikum verejooks liigestesse, lihastesse või hematoomi: 30–60% normaalsest, korrake infusioone iga 12–24 tunni järel 3-4 päeva või kauem, kuni valu ja funktsioon taastuvad. Eluohtlik verejooks: 60–100% normaalsest, korrake infusioone iga 8–24 tunni järel, kuni oht on lahenenud. Väike operatsioon, sealhulgas hamba väljatõmbamine: 30–60% normist iga 24 tunni järel, vähemalt 1 päev, kuni haav on paranenud. Suuroperatsioon: 80–100% normaalsest (enne ja pärast operatsiooni), korrake infusioone iga 8–24 tunni järel, kuni haav on piisavalt paranenud, seejärel jätkake ravi vähemalt 7 järjestikust päeva, et säilitada VIII faktori aktiivsus 30 ° C juures -60%. Pidev infusioon: hinnanguline kliirens tuleb arvutada enne operatsiooni. Esialgse infusioonikiiruse saab arvutada järgmiselt: kliirens x soovitud püsikontsentratsioon = infusioonikiirus (RÜ / kg / h). Pärast esimest 24 tundi pidevat infusiooni tuleb kliirens iga päev uuesti arvutada, kasutades tahke oleku valemit koos mõõdetud kontsentratsiooni ja teadaoleva infusioonikiirusega. Annuse arvutamiseks ja infusioonide sageduse määramiseks on vajalik VIII faktori plasmataseme regulaarne määramine. Raske A-hemofiiliaga patsientide verejooksu pikaajaliseks profülaktikaks tuleb manustada VIII faktori annus 20–40 RÜ. faktor VIII / kg 2-3-päevaste vahedega.
Näidustused
Verejooksu ravi ja profülaktika A-hemofiilia (kaasasündinud VIII faktori defitsiit) patsientidel. Ravim ei sisalda farmakoloogiliselt efektiivset kogust von Willebrandi faktorit ja seetõttu ei saa seda kasutada von Willebrandi haiguse ravis.
Vastunäidustused
Ülitundlikkus toimeaine või ravimi mis tahes koostisosade suhtes.
Ettevaatusabinõud
Kui ilmnevad ülitundlikkusnähud, lõpetage viivitamatult preparaadi kasutamine. Inimese verest või plasmapreparaatidest põhjustatud nakkuse ennetamise standardsed meetodid hõlmavad doonorite valimist, üksikute annetuste ja plasmakogumite testimist konkreetsete infektsioonimarkerite suhtes ning tõhusate tootmismeetodite kasutamist viiruste inaktiveerimiseks / eemaldamiseks. Sellest hoolimata ei saa inimverest või -plasmast valmistatud ravimite manustamisel täielikult välistada nakkusetekitajate edasikandumise võimalust. See kehtib ka tundmatute või tekkivate viiruste ja muude patogeenide kohta. Kasutatavaid meetodeid peetakse tõhusaks ümbrisega viiruste nagu HIV, HBV ja HCV vastu ning neil võib olla piiratud väärtus ümbrisega viiruste nagu HAV ja parvoviirus B19 vastu (võivad olla ohtlikud rasedatele ja immuunpuudulikkuse või liigse erütropoeesi põdevatele naistele). Piisavad vaktsineerimised (A- ja B-hepatiidi vastu) on näidustatud patsientidel, kes saavad regulaarset või korduvat ravi inimese VIII hüübimisfaktoriga. VIII faktori neutraliseerivate antikehade (inhibiitorite) tekkimine on teadaolev komplikatsioon A-hemofiiliaga patsientide ravimisel - patsiente tuleb asjakohaste kliiniliste vaatluste ja laboratoorsete testide abil jälgida inhibeerivate antikehade tekke suhtes. Kirjanduses on teatatud korrelatsioonist VIII faktori inhibiitorite esinemise ja allergiliste reaktsioonide vahel. Patsientidel, kellel tekivad allergilised reaktsioonid, tuleb inhibiitorit testida VIII faktori poolt indutseeritud anafülaksia suurenenud riski tõttu. Allergiliste reaktsioonide ohu tõttu tuleb VIII faktori esmakordne manustamine läbi viia raviarsti äranägemisel, arsti järelevalve all kohas, kus on võimalik pakkuda allergilise reaktsiooni korral piisavat meditsiinilist abi. Ravim sisaldab naatriumi - 1 viaal 250 RÜ Sisaldab vähem kui 1 mmol (23 mg) naatriumi, see tähendab, et see annus on põhimõtteliselt „naatriumivaba“ ja 1 viaal 500 RÜ. või 1000 RÜ Sisaldab kuni 1,75 mmol (40 mg) naatriumi, mida tuleb arvestada naatriumisisaldusega dieedil olevatel patsientidel.
Soovimatu tegevus
Harv: ülitundlikkusreaktsioonid, palavik, veres esinevad VIII faktori vastased antikehad. Väga harv: anafülaktiline šokk.
Rasedus ja imetamine
Kuna naistel esineb harva A-hemofiiliat, pole VIII faktori kasutamise kohta raseduse ja imetamise ajal kogemusi. Seetõttu võib VIII faktorit raseduse ja imetamise ajal manustada ainult rangelt näidustatud juhtudel.
Koostoimed
Puuduvad teadaolevad inimese VIII hüübimisfaktori preparaatide koostoimed teiste ravimitega.
Preparaat sisaldab ainet: VIII faktor
Kompenseeritud ravim: EI

.jpg)