Keegi ei näi kahtlevat, et inimese, eriti soolestiku, mikrobiootol on tervises määrav roll. Teadmised inimkeha selle mikrobioloogilise organi kohta ei saanud aga algust enne genoomiajastu algust. Seetõttu, nagu on juhtunud inimese genoomiga, tehakse tõelised avastused endise nimega bakteriaalse floora potentsiaalist siis, kui kõik sellised algatused nagu Human Microbiome Project saadud andmed on korralikult töödeldud ja geenid valkudele üle antud .
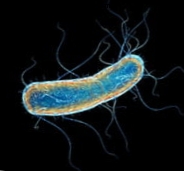
Mikrobiota on tundmatu sõber. See on inimkonda saatnud aegade algusest peale ja selle olulisust on juba ammu tunnustatud. Ukraina mikrobioloog Ilja Mechnikov (1845-1906) tegi 1908. aastal ettepaneku, et bakterite allaneelamine võib positiivselt mõjutada seedetrakti normaalset mikrofloorat. Samuti püstitas ta hüpoteesi, et laktobatsillid on olulised inimese tervisele.
Alates Mechnikovi ajast on mikrobiota uurimisel tehtud edusamme tilgutite abil. Lisaks on suurem osa leidudest koondunud viimastesse aastatesse: PubMedis alates 1977. aastast registreeritud 1600 soolestiku mikrobiotot käsitlevast publikatsioonist avaldati 2011. aastal peaaegu kolmandik.
Selle valdkonna töö hüppeline kasv on selgitanud mõnda olulist küsimust. Näiteks on kinnitatud, et mitmed mikrobiotabakterite liigid on võimelised metaboliseerima süsivesikuid, mida inimese soolestik ei suuda seedida. On ka liike, mis toodavad kasulikke vitamiine ja mineraale neile, kes neid võõrustavad.
Veel pole selge, kas seedesüsteemil ei olnud kunagi geene, mis kodeerivad nende funktsioonide eest vastutavaid ensüüme, või kaotasid nad evolutsiooni käigus, kuna mikroorganismid võtsid need ülesanded endale.
Iduvabade hiirtega tehtud uuringud on näidanud, et on võimalik elada ka ilma soolestiku mikrobiotata, kuid peate maksma väga kõrget hinda, kuna katseloomad vajavad terveks ja piisava raskusega püsimiseks suurt hulka ja mitmekesist toitaineid.
Keegi ei kahtle tugevas seos, mis eksisteerib organismis elava bakterikommuuni ja tervise vahel tänu selle mõjule immuunvastusele, seedimisele ja isegi neuroloogilistele protsessidele. Põhjus-tagajärg seos pole aga siiani teada. Kas mikrobiota koostis peegeldab lihtsalt inimese toitumist või on see tegur, mis mõjutab aktiivselt tema tervist? Kas mikrobiota muutuste esilekutsumist saaks kasutada teatud haiguste raviks?
On märke, et ärritunud soole sündroom, haavandiline koliit või Crohni tõbi võivad olla seotud bakteriaalse floora tasakaalustamatusega. Siiski pole veel teada, kas need erinevused mikrobiota koostises ja metaboolses aktiivsuses on nende haiguste otsesed põhjused või on nendega seotud protsessid.
Eksperdid, kes hiljuti osalesid Evianis (Prantsusmaal) peetud esimesel tervisekontrolli teemal soolte mikrobiota tervise alal, usuvad, et mikrobiota modifikatsioonil põhinevate terapeutiliste rakenduste täielikuks sisenemiseks on veel liiga vara.
Üks tippkohtumisel osalenutest, Barcelona Valle de Hebroni haigla teadur ja Hispaania probiootikumide ja prebiootikumide seltsi president Francisco Guarner selgitab mikrobiota uurimisega viivitamise peamist põhjust: "Traditsioonilised meetodid bakterite uurimiseks olid nakkushaiguste korral väga head, kuna nende nakatatud bakteritel on üldiselt suurem genoom ja suuremad ressursid, nii et neid saab kasvatada.
Kuid aastail 1999-2000 nägid teadlased soolestiku baktereid mikroskoobi all, kuid ei suutnud neid nimetada, kuna nad ei saanud kasvada. "Geneetilise järjestuse määramise tehnika ja arvutiandmete töötlemine on maastikku muutnud. Kõigis bakterites esinevat geeni 16S on kasutatud organismi erineva mikrobiota elanike taksonoomias (soolestiku, naha, suu kaudu ...) Samuti on sekveneeritud arvukate bakterite täielikud genoomid.
Bakterite suur mitmekesisus saab teada. Praeguseks on tuvastatud enam kui neli miljonit erinevat bakterigeeni ja teadaolevalt kannab iga inimene umbes 600 000. Rahvusvahelistest algatustest nagu Human Microbiome Project või MetaHIT konsortsium (inimese sooletrakti metageneetika) loodud avalikud andmebaasid hakkavad vilja kandma.
Teadlased väldivad võidukäiku, mis võib vallandada tohutu hulga andmeid, mis on tänu rahvusvahelistele projektidele kogutud väga lühikese aja jooksul. James Versalovic, Baylori meditsiinikoolist (Ameerika Ühendriigid) ja projekti Human Microbiome liige, juhib tähelepanu, et praegusel ajal on nad hakanud "mõistma mikrobiomi funktsioone. Paljusid jagavad erinevad indiviidid, teised aga mitte." Samuti on tõestatud, et haigusega on seotud väiksema mitmekesisusega bakterid. Nüüd on veel hea viis tervikliku mõistatuse rekonstrueerimiseks. "DNA andmed on meil olemas, kuid meil pole endiselt palju RNA-teavet. See on järgmine samm, " ütleb ta.
Hispaanias MetaHIT-i eest vastutav Guarner juhib tähelepanu, et "on palju haigusi, mida inimese genoom ei seleta, ja tõenäoliselt peame kogu pildi saamiseks ja nende mõistmiseks ekstraheerima andmed inimese mikrobiomist." Nende patoloogiate hulgas on rasvumine, II tüüpi diabeet, põletikulised haigused, astma ja allergiad. Dieet, hügieeniteooria ja mikrobiota mängivad kõigis nendes tõenäoliselt otsustavat rolli. Kuid palju on veel uurimata.
On kinnitatud, et mitmed bakteriliigid suudavad metaboliseerida süsivesikuid, mida inimese soolestik ei suuda seedida
Väiksemat bakterite mitmekesisust seostatakse haiguste esinemisega, kuid pole veel täpselt teada, milline on põhjuslik seos
Iga inimene kannab umbes 25 000-30 000 inimese geeni ja 600 000 mikroobi geeni.
Iga inimese soolestiku mikrobiotot moodustavate mikroorganismide kooslus sisaldab vähemalt 1014 bakterit, mis kaaluvad koos 1, 5–2 kg.
On tuvastatud enam kui 1000 erinevat bakteriliiki, kuid usutakse, et mitmekesisus on palju suurem.
Kolm serva moodustavad umbes 75% mitmekesisusest: mikroorganismid, bakteroidid ja aktinobakterid.
Soolestiku mikrobiootad võib vastavalt domineerivatele bakteritele jagada kolmeks suureks rühmaks või enterotüübiks: Bacteroides, Prevotella ja Ruminococcus.
Ligi kolmandik soolefloora väljaannetest, mis on avaldatud alates 1977. aastast, ilmus 2011. aastal.
Viimastel aastatel on alustatud doonori väljaheidetega mikrobiota siirdamist. Selle ravi paljutõotavad tulemused on kajastunud peamiselt Clostridium difficile infektsiooniga patsientidel. "Huvi selle teraapia vastu on ajendatud uutest uuringutest soole mikrobiota kohta, mida hakatakse täheldama inimese bakteriaalse elundina, millel on olulised funktsioonid energia metabolismis ja immuunsuses, " kirjeldavad selle ülevaate autorid protseduur, mis avaldati eelmise aasta detsembris ajakirjas Nature Reviews Gastroenterology and Hepatology. James Versalovic leiab, et see on pisut konkreetne protseduur: "Küsimus on selles, kas haigusi põhjustavad bakterid või viirused võivad edasi kanduda ka fekaalide kaudu." Probiootikumid ja dieedimuudatused kujutaksid endast ohutumat terapeutilist sekkumist, kuid nende tegeliku potentsiaali kohta oleme alles teadmise alguses.
Allikas:
Silte:
Dieet-Ja Toitumise Ilu Tervis
Mikrobiota on tundmatu sõber. See on inimkonda saatnud aegade algusest peale ja selle olulisust on juba ammu tunnustatud. Ukraina mikrobioloog Ilja Mechnikov (1845-1906) tegi 1908. aastal ettepaneku, et bakterite allaneelamine võib positiivselt mõjutada seedetrakti normaalset mikrofloorat. Samuti püstitas ta hüpoteesi, et laktobatsillid on olulised inimese tervisele.
Alates Mechnikovi ajast on mikrobiota uurimisel tehtud edusamme tilgutite abil. Lisaks on suurem osa leidudest koondunud viimastesse aastatesse: PubMedis alates 1977. aastast registreeritud 1600 soolestiku mikrobiotot käsitlevast publikatsioonist avaldati 2011. aastal peaaegu kolmandik.
Selle valdkonna töö hüppeline kasv on selgitanud mõnda olulist küsimust. Näiteks on kinnitatud, et mitmed mikrobiotabakterite liigid on võimelised metaboliseerima süsivesikuid, mida inimese soolestik ei suuda seedida. On ka liike, mis toodavad kasulikke vitamiine ja mineraale neile, kes neid võõrustavad.
Veel pole selge, kas seedesüsteemil ei olnud kunagi geene, mis kodeerivad nende funktsioonide eest vastutavaid ensüüme, või kaotasid nad evolutsiooni käigus, kuna mikroorganismid võtsid need ülesanded endale.
Iduvabade hiirtega tehtud uuringud on näidanud, et on võimalik elada ka ilma soolestiku mikrobiotata, kuid peate maksma väga kõrget hinda, kuna katseloomad vajavad terveks ja piisava raskusega püsimiseks suurt hulka ja mitmekesist toitaineid.
Põhjus või tagajärg?
Keegi ei kahtle tugevas seos, mis eksisteerib organismis elava bakterikommuuni ja tervise vahel tänu selle mõjule immuunvastusele, seedimisele ja isegi neuroloogilistele protsessidele. Põhjus-tagajärg seos pole aga siiani teada. Kas mikrobiota koostis peegeldab lihtsalt inimese toitumist või on see tegur, mis mõjutab aktiivselt tema tervist? Kas mikrobiota muutuste esilekutsumist saaks kasutada teatud haiguste raviks?
On märke, et ärritunud soole sündroom, haavandiline koliit või Crohni tõbi võivad olla seotud bakteriaalse floora tasakaalustamatusega. Siiski pole veel teada, kas need erinevused mikrobiota koostises ja metaboolses aktiivsuses on nende haiguste otsesed põhjused või on nendega seotud protsessid.
Taksonoomia
Eksperdid, kes hiljuti osalesid Evianis (Prantsusmaal) peetud esimesel tervisekontrolli teemal soolte mikrobiota tervise alal, usuvad, et mikrobiota modifikatsioonil põhinevate terapeutiliste rakenduste täielikuks sisenemiseks on veel liiga vara.
Üks tippkohtumisel osalenutest, Barcelona Valle de Hebroni haigla teadur ja Hispaania probiootikumide ja prebiootikumide seltsi president Francisco Guarner selgitab mikrobiota uurimisega viivitamise peamist põhjust: "Traditsioonilised meetodid bakterite uurimiseks olid nakkushaiguste korral väga head, kuna nende nakatatud bakteritel on üldiselt suurem genoom ja suuremad ressursid, nii et neid saab kasvatada.
Kuid aastail 1999-2000 nägid teadlased soolestiku baktereid mikroskoobi all, kuid ei suutnud neid nimetada, kuna nad ei saanud kasvada. "Geneetilise järjestuse määramise tehnika ja arvutiandmete töötlemine on maastikku muutnud. Kõigis bakterites esinevat geeni 16S on kasutatud organismi erineva mikrobiota elanike taksonoomias (soolestiku, naha, suu kaudu ...) Samuti on sekveneeritud arvukate bakterite täielikud genoomid.
Bakterite suur mitmekesisus saab teada. Praeguseks on tuvastatud enam kui neli miljonit erinevat bakterigeeni ja teadaolevalt kannab iga inimene umbes 600 000. Rahvusvahelistest algatustest nagu Human Microbiome Project või MetaHIT konsortsium (inimese sooletrakti metageneetika) loodud avalikud andmebaasid hakkavad vilja kandma.
Tulevik
Teadlased väldivad võidukäiku, mis võib vallandada tohutu hulga andmeid, mis on tänu rahvusvahelistele projektidele kogutud väga lühikese aja jooksul. James Versalovic, Baylori meditsiinikoolist (Ameerika Ühendriigid) ja projekti Human Microbiome liige, juhib tähelepanu, et praegusel ajal on nad hakanud "mõistma mikrobiomi funktsioone. Paljusid jagavad erinevad indiviidid, teised aga mitte." Samuti on tõestatud, et haigusega on seotud väiksema mitmekesisusega bakterid. Nüüd on veel hea viis tervikliku mõistatuse rekonstrueerimiseks. "DNA andmed on meil olemas, kuid meil pole endiselt palju RNA-teavet. See on järgmine samm, " ütleb ta.
Hispaanias MetaHIT-i eest vastutav Guarner juhib tähelepanu, et "on palju haigusi, mida inimese genoom ei seleta, ja tõenäoliselt peame kogu pildi saamiseks ja nende mõistmiseks ekstraheerima andmed inimese mikrobiomist." Nende patoloogiate hulgas on rasvumine, II tüüpi diabeet, põletikulised haigused, astma ja allergiad. Dieet, hügieeniteooria ja mikrobiota mängivad kõigis nendes tõenäoliselt otsustavat rolli. Kuid palju on veel uurimata.
On kinnitatud, et mitmed bakteriliigid suudavad metaboliseerida süsivesikuid, mida inimese soolestik ei suuda seedida
Väiksemat bakterite mitmekesisust seostatakse haiguste esinemisega, kuid pole veel täpselt teada, milline on põhjuslik seos
Joonistel
Iga inimene kannab umbes 25 000-30 000 inimese geeni ja 600 000 mikroobi geeni.
Iga inimese soolestiku mikrobiotot moodustavate mikroorganismide kooslus sisaldab vähemalt 1014 bakterit, mis kaaluvad koos 1, 5–2 kg.
On tuvastatud enam kui 1000 erinevat bakteriliiki, kuid usutakse, et mitmekesisus on palju suurem.
Kolm serva moodustavad umbes 75% mitmekesisusest: mikroorganismid, bakteroidid ja aktinobakterid.
Soolestiku mikrobiootad võib vastavalt domineerivatele bakteritele jagada kolmeks suureks rühmaks või enterotüübiks: Bacteroides, Prevotella ja Ruminococcus.
Ligi kolmandik soolefloora väljaannetest, mis on avaldatud alates 1977. aastast, ilmus 2011. aastal.
PROBIOTIKAST TRANSPORTIDELE
Viimastel aastatel on alustatud doonori väljaheidetega mikrobiota siirdamist. Selle ravi paljutõotavad tulemused on kajastunud peamiselt Clostridium difficile infektsiooniga patsientidel. "Huvi selle teraapia vastu on ajendatud uutest uuringutest soole mikrobiota kohta, mida hakatakse täheldama inimese bakteriaalse elundina, millel on olulised funktsioonid energia metabolismis ja immuunsuses, " kirjeldavad selle ülevaate autorid protseduur, mis avaldati eelmise aasta detsembris ajakirjas Nature Reviews Gastroenterology and Hepatology. James Versalovic leiab, et see on pisut konkreetne protseduur: "Küsimus on selles, kas haigusi põhjustavad bakterid või viirused võivad edasi kanduda ka fekaalide kaudu." Probiootikumid ja dieedimuudatused kujutaksid endast ohutumat terapeutilist sekkumist, kuid nende tegeliku potentsiaali kohta oleme alles teadmise alguses.
Allikas: